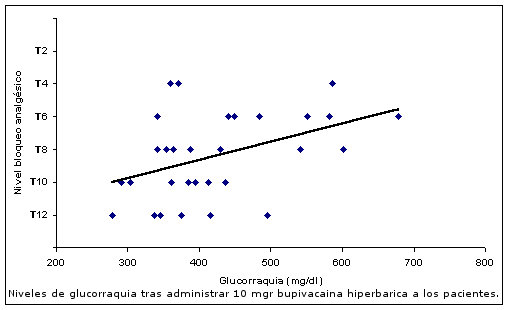
La dirección de la línea indica que en general después de la administración de bupivacaína hiperbárica en el LCR, a mayor nivel de glucorraquia se corresponde un nivel mas alto de analgesia.
Mecanismo de acción de la bupivacaína hiperbárica en la raquianestesia.
Bupivacaína hiperbárica.
La anestesia raquídea comienza en 1885 fecha en que fue practicada por primera vez por J. Leonard Corning en New York. Desde el inicio de utilización de esta técnica con el objetivo de dirigir su efecto, se aumentaba la baricidad de la solución anestésica añadiéndole glucosa a distintas concentraciones, esto incrementa la glucorraquia en el LCR de forma temporal. El anestésico más utilizado actualmente es la bupivacaína hiperbárica.
Aunque la raquianestesia es un método catalogado dentro de la Anestesia Loco-Regional, se diferencia de los procedimientos de Anestesia Local como los Bloqueos nerviosos, en que el anestésico (en nuestro medio bupivacaína hiperbárica) se introduce en el espacio raquìdeo y el tejido nervioso incluído en su interior (neuronas motoras, sensitivas, autónomas y sistema de conducción) inmersos en el LCR, carece de membranas protectoras y de mielina, con lo que su efecto es rápido y además puede originar un efecto sistémico importante.
Así, aunque la cantidad de anestésico necesario para llevar a cabo una intervención de herniorrafia, prostatectomía, safenectomía ó intervenciones de rodilla o cadera es escaso (2 ó 3 ml de bupivacaína al 0,5 % son suficientes), el efecto causado puede ser devastador, no son infrecuentes caídas importantes de la presión arterial, de la frecuencia cardíaca, en suma del gasto cardíaco, con afectación de los músculos respiratorios, que conducen incluso a la parada cardio-respiratoria.
El riesgo aumenta sobre todo en embarazadas (cesáreas), obesos o en caso de tumores que compriman la cava. En todos estos casos está dificultado el retorno venoso, disminuye el calibre del canal raquídeo y el volumen de LCR. Esto último aumenta la altura alcanzada de anestesia1 y los efectos secundarios de esta técnica, pues se incrementa el bloqueo del sistema nervioso simpático y de los nervios que inervan los músculos respiratorios.
Tanto es así, que la realización de una raquianestesia precisa de la preparación de sustancias vasoconstrictoras y cardioprotectoras (efedrina y atropina), siendo los anestesiólogos expertos en el manejo seguro y adecuado de estas sustancias, no exentas a su vez de efectos secundarios.
Todo lo anterior, es conocido por los anestesiólogos, pero existen aspectos no bien investigados de esta técnica o que pasan desapercibidos. Uno es la composición de la solución anestésica utilizada habitualmente cuando se realiza este procedimiento, que es la bupivacaína hiperbárica que contiene bupivacaín al 0,5 % y glucosa al 8,25% (8.250 mg dL-1). Esta cantidad es 100 veces la cantidad de glucosa que existe normalmente en el LCR (50-80 mg dL-1). Esto la convierte en una solución muy pesada que hace que se desplace siguiendo los cambios posturales, incluso si después de 20 a 60 minutos de haberla administrado y de mantener al paciente en posición sentada, se pasa a la posición supina, la extensión del efecto anestésico sigue modificándose con el cambio postural. Esto parece indicar que incluso después de 60 minutos la glucosa puede seguir dirigiendo el sentido del efecto anestésico de la bupivacaína.
Este fenómeno2 puede ser debido a que la glucosa de la solución de bupivacaína hiperbárica está unida mediante enlaces de hidrógeno a las moléculas de agua del LCR. El clorhidrato de bupivacaína se disuelve en el agua de la disolución en la que se encuentra gracias a las atracciones electrostáticas que surgen entre los dipolos del agua y los iones bupivacaína-H+ y cloruro (Cl–), formándose los correspondientes iones hidratados muy estables, de manera que se supera la tendencia de los primeros a atraerse mutuamente y la sal de bupivacaína queda así rodeada simétricamente por moléculas de agua. Éste fenómeno recibe el nombre de solvatación. Las moléculas de glucosa hidratadas impiden que los iones hidratados de bupivacaína puedan moverse libremente en el seno de la disolución. Así, la bupivacaína y la glucosa, le confieren a ésta solución anestésica su elevada densidad, superior a la del LCR.
Este hecho de la alta concentración de glucosa debido a la administración de bupivacaína hiperbárica, no es bien entendido habitualmente. Los correctores de los artículos que tratan sobre este asunto2,3 insisten en resaltar la relevancia de los pacientes diabéticos en las cifras de glucorraquia. Y reiteradamente se ha de explicar la irrelevancia de que un sujeto presente en su glucorraquia basal 10 ó 20 mg por encima de lo habitual, cuando en las mediciones1,2 a los 5, 10, 15 y 20 minutos, las cifras medias de glucorraquia eran en los enfermos estudiados de: 1027,07± 349,04 mg dL-1, 416,35 ± 88,24 mg dL-1, 388,07 ± 83,72 mg dL-1 y 364,73 ± 75,90 mg dL-1. Las media de la glucorraquia basal eran de: 65,93 ± 10,48 mg dL-1. Figura 1.
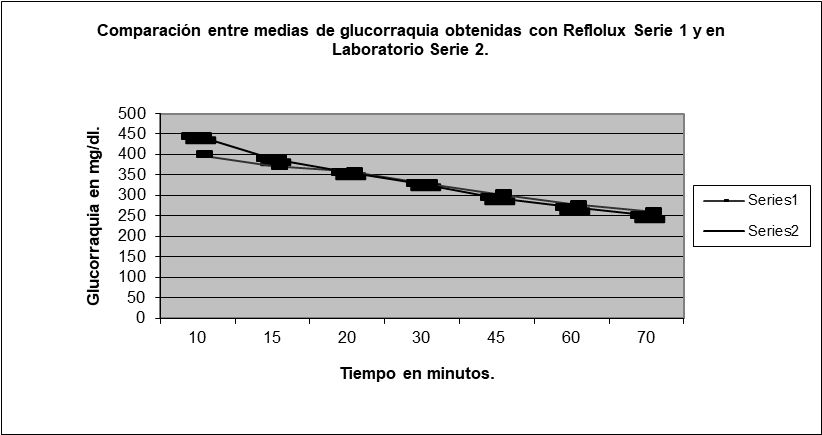
Figura 1-. Se observa como las cifras de glucorraquia en distintos períodos de tiempo, obtenidas tras la administración de 10 mgr de bupivacaína hiperbárica a una serie de pacientes intervenidos bajo raquianestesia y analizadas con un Glucómetro y en el Laboratorio van disminuyendo.
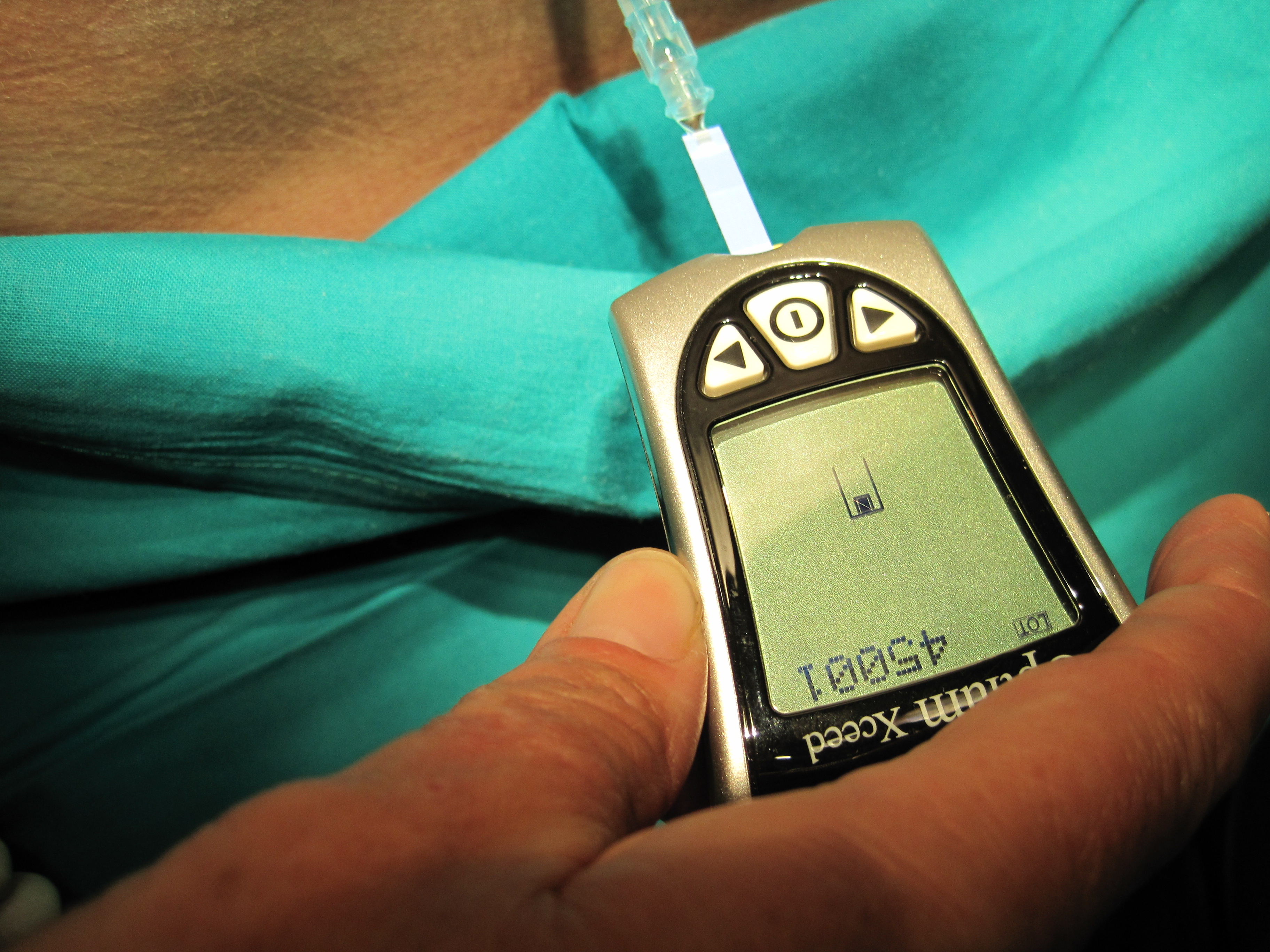
Figura 2.-Análisis de la glucorraquia con un glucómetro, analizando una gota de LCR obtenida tras la punción lumbar. La colocación de la tira reactiva en el instrumento se ha realizado aplicando medidas asépticas.
Tampoco está muy difundido no sólo entre los anestesiólogos sino también entre los médicos internistas que con un glucómetro4 (Fig 2) se puede analizar la glucorraquia sin necesidad de trasladar la muestra al Laboratorio del Hospital.
Como se observa en la imagen de entrada en el eje de ordenadas las cifras más bajas de vertebras torácicas son las mas alejadas del origen, esto conviene tenerlo en cuenta cuando se realizan estos gráficos para no dar lugar a confusiones con los resultados, que en distintos trabajos pueden resultar contradictorios. También se comprueba que en general a mayor nivel de glucorraquia, se corresponde un nivel más alto de bloqueo analgésico.
Bibliografía.-
1.-http://www.mianestesia.es/dilucion-de-la-glucorraquia/
2.-Sánchez Morillo J, Demartini Ferrari A, Estañ Capell N, Viñals Bellido P, Quiñiones Torrelo C, Morales Suárez-Valera. Relation between glucose concentrations in cerebrospinal fluid and sensory and motor block during spinal anesthesia with hyperbaric bupivacaine. Rev Esp Anestesiol Reanim. 2006 Jan;53(1):11-7. [Article in Spanish].
3.-Estañ-Capell N, Quiñones-Torrelo C, Sánchez-Morillo J, Estañ-Jago L. Correlation between glucose and bupivacaine levels in cerebrospinal fluid after spinal anesthesia: glycorrhachia as predictor for duration of sensory block. Clin Chem Lab Med. 2010 Apr;48(4):523-30. doi: 10.1515/CCLM.2010.094.
4.- Sánchez Morillo J, Soliveres Ripoll J, Estañ Capell N, Solaz Roldán C, Viñals Bellido P, Quiñones Torrelo C. Comparison of 2 devices to measure spinal fluid glucose concentration in hyperbaric spinal anesthesia. Rev Esp Anestesiol Reanim. 2007 Feb;54(2):73-7.
